- Pubblicazione il 30 Settembre 2024
Introduzione
Le micosi broncopolmonari allergiche rappresentano un gruppo di patologie respiratorie caratterizzate da una risposta immunitaria anomala verso funghi ambientali, in particolare Aspergillus sp. Queste condizioni si verificano in pazienti affetti da condizioni predisponenti, e principalmente in presenza di malattie polmonari sottostanti come asma o fibrosi cistica. Tali micosi broncopolmonari allergiche possono comportare un significativo deterioramento della funzione polmonare e della qualità della vita.
La necessità di nuove linee guida per la gestione delle micosi broncopolmonari allergiche è emersa in risposta alla crescita della conoscenza scientifica e clinica su queste condizioni. Ricerche recenti hanno chiarito diversi aspetti cruciali riguardanti la patogenesi, la diagnosi precoce e le opzioni di trattamento più efficaci.
Le precedenti linee guida del 2013, sebbene fornissero raccomandazioni utili, presentavano numerosi punti deboli. Innanzitutto, la classificazione delle micosi broncopolmonari allergiche era limitata, e non considerava adeguatamente le varianti cliniche e le risposte individuali ai trattamenti. Mancava anche una discussione dettagliata sui biomarcatori recentemente identificati, che sono fondamentali per una diagnosi differenziale accurata e mirata. Il trattamento allora consigliato era centrato prevalentemente sull'uso di corticosteroidi sistemici, senza che fossero forniti sufficienti orientamenti su terapie addizionali o alternative, come gli antifungini o le terapie biologiche. Inoltre, le raccomandazioni per il monitoraggio a lungo termine dei pazienti erano poco chiare, e rendevano difficile l'adattamento della terapia in base alla risposta clinica.
Pertanto, il presente articolo si propone di esaminare le novità introdotte dalle recenti linee guida dell’ISHAM-ABPA working group, evidenziando gli aggiornamenti critici e le implicazioni cliniche che derivano dall'evidenza emergente in questo campo.
Novità
Le nuove linee guida del 2024 offrono una revisione sostanziale delle precedenti raccomandazioni risalenti al 2013, affrontando vari aspetti clinici cruciali. Di seguito presentiamo un'analisi approfondita delle migliorie introdotte, organizzata per argomenti chiave.
1. Classificazioni
1a) Nomenclatura
Gli esperti hanno ritenuto innanzitutto necessario distinguere anche dal punto di vista terminologico due principali entità clinico-patologiche. Nello specifico, oltre alla nota aspergillosi broncopolmonare allergica (ABPA, condizione nella quale la micosi allergica è causata da un fungo della specie Aspergillus), viene introdotto il concetto di micosi broncopolmonare allergica (ABPM). L’ABPM è una condizione molto meno comune attribuibile alla colonizzazione da parte di funghi non appartenenti alla specie Aspergillus; i microrganismi più frequentemente responsabili includono Bipolaris spp, Schizophullum spp, Curvularia spp e Candida Albicans. La chiara differenziazione tra ABPA e ABPM permette ai clinici di adottare strategie di trattamento più mirate. Infatti, saper distinguere tra queste due condizioni è cruciale per eseguire una diagnostica e una gestione adeguata, evitando sovrapposizioni terapeutiche e migliorando gli esiti clinici per i pazienti affetti.
1b) Classificazione clinica
La classificazione clinica dell’ABPA è di fondamentale importanza in considerazione delle numerose riacutizzazioni che fanno parte della storia di malattia e della probabilità di sviluppare nel tempo complicanze severe. In passato la patologia veniva suddivisa in sei stadi, che tuttavia non riflettevano la severità della malattia. L’ISHAM-AWG ha dunque proposto una nuova classificazione in cui vengono descritte cinque categorie: ABPA acuta, Risposta, Remissione, ABPA dipendente dal trattamento, ABPA avanzata.
|
ABPA acuta |
Nuova diagnosi: ABPA/M precedentemente non diagnosticata, rientrante nei criteri diagnostici Esacerbazione in paziente con diagnosi di ABPA/M: Riacutizzazione infettiva/bronchiectasica: peggioramento clinico sostenuto per almeno 48 ore con incremento di tosse, dispnea, volume/consistenza dell’espettorato, espettorato purulento, astenia, febbre o emottisi in assenza di evidenza immunologica o radiologica di deterioramento di ABPA/M |
|
Risposta |
- Miglioramento della sintomatologia di almeno il 50% (su Likert o Visual Analogic Scale); e |
|
Remissione |
- Miglioramento clinico-radiologico sostenuto per almeno 6 mesi senza trattamento corticosteroideo; e - Assenza di rialzo delle IgE totali sieriche di ³ 50% rispetto all’ultimo valore registrato durante stabilità clinica |
|
ABPA dipendente dal trattamento |
- Due o più esacerbazioni di ABPA/M consecutive nell’arco di 3 mesi dalla sospensione della terapia corticosteroidea - Peggioramento dei sintomi clinici e peggioramento radiologico o incremento delle IgE sieriche totali del 50% nell’arco di 4 settimane dal tapering della terapia corticosteroidea in due occasioni separate |
|
ABPA avanzata |
- Bronchiectasie estese a ³ 10 segmenti secondarie ad ABPA/M all’imaging toracico; e |
Tabella 1 – Raccomandazioni del gruppo di lavoro Revised International Society for Human and Animal Mycology (ISHAM)-ABPA per la classificazione clinica e i criteri di risposta al trattamento di ABPA/M
1c) Classificazione radiologica
Dopo la discussione di numerose opzioni, il gruppo di lavoro ha delineato la nuova classificazione radiologica che include cinque classi: ABPA sierologica (ABPA-S), ABPA con bronchiectasie (ABPA-B), ABPA con tappi mucosi (ABPA-MP), ABPA con muco ad alta attenuazione (ABPA-HAM) e ABPA con fibrosi pleuropolmonare cronica (ABPA-CPF).
|
ABPA-S |
ABPA senza bronchiectasie |
|
ABPA-B |
ABPA con evidenza radiologica di bronchiectasie |
|
ABPA-MP |
ABPA con tappi mucosi ma senza muco ad alta attenuazione; pazienti con bronchiectasie e concomitanti tappi mucosi verranno classificati come ABPA-MP |
|
ABPA-HAM |
ABPA con muco ad alta attenuazione |
|
ABPA-CPF |
ABPA con due o più dei seguenti: fibrosi polmonare, lesioni fibro-cavitarie, aspergilloma e ispessimento pleurico |
Tabella 2 – Raccomandazioni del gruppo di lavoro Revised International Society for Human and Animal Mycology (ISHAM)-ABPA per la classificazione radiologica di ABPA/M
2. Diagnosi
La revisione dei criteri diagnostici per l'ABPA nelle linee guida ISHAM-ABPA 2024 ha comportato diversi cambiamenti significativi rispetto alle precedenti linee guida del 2013.
I nuovi criteri richiedono un approccio multidimensionale alla patologia: è infatti necessario ai fini della conferma diagnostica dimostrare un incremento delle IgE sieriche totali (con nuovo cut-off ³ 500 UI/mL) e Aspergillo-specifiche, associato ad altre componenti tra cui sono compresi IgG sieriche fungo-specifiche, ipereosinofilia periferica e un quadro radiologico compatibile con ABPA.
Sono stati dunque introdotti nuovi biomarcatori tra cui assumono un ruolo fondamentale ai fini diagnostici le IgE specifiche per Aspergillus, dimostratesi maggiormente sensibili rispetto ai precedentemente impiegati test cutanei. Inoltre, la determinazione delle IgG specifiche contro Aspergillus tramite immunoassay enzimatico si è dimostrata superiore all’immunoprecipitazione.
|
|
ABPA |
ABPM |
|
Condizioni predisponenti |
- Asma, fibrosi cistica, patologia polmonare ostruttiva cronica, bronchiectasie; o |
- Asma, fibrosi cistica, patologia polmonare ostruttiva cronica, bronchiectasie; o |
|
Componenti essenziali |
- IgE specifiche per A.fumigatus ³ 0.35 kUA/L |
- IgE fungo-specifiche elevate - IgE totali sieriche ³ 500 UI/mL |
|
Altri componenti (almeno due) |
- IgG per A.fumigatus positive - TC torace ad alta risoluzione compatibile con ABPA o opacità transitorie a Rx torace compatibili con ABPA |
- IgG fungo-specifiche positive - eosinofilia periferica ³ 500 cell/microL (anche precedente alla valutazione) - Due esami colturali dell’espettorato (o un lavaggio broncoalveolare) con crescita del fungo causativo - TC torace ad alta risoluzione compatibile con ABPA o opacità transitorie a Rx torace compatibili con ABPA |
Tabella 3 – Consensus del gruppo di lavoro Revised International Society for Human and Animal Mycology (ISHAM)-ABPA sui criteri diagnostici di ABPA/M
3. Trattamento
3a) Trattamento dell’ABPA di nuova diagnosi e delle esacerbazioni
In caso di ABPA acuta di nuovo riscontro è raccomandato trattamento per via orale con prednisolone a dosaggio basso-moderato (0.5 mg/kg/die) per 2-4 settimane, da scalare gradualmente fino a completa sospensione nell’arco di 4 mesi o con itraconazolo per 4 mesi. Lo stesso approccio terapeutico è raccomandato anche per i casi di esacerbazione acuta. Il consensus non raccomanda l’impiego di terapia sistemica per casi di ABPA asintomatica; per quanto concerne l’ABPA-S, è invece suggerito l’avvio del trattamento solo nei casi in cui vi sia uno scarso controllo dell’asma o in caso di frequenti riacutizzazioni nonostante terapia inalatoria in atto. L’associazione di prednisolone e itraconazolo è indicata solamente in caso di esacerbazioni ricorrenti (almeno 2 riacutizzazioni negli ultimi 1-2 anni).
3b) Monitoraggio della risposta al trattamento
Il gruppo di lavoro raccomanda di verificare l’iniziale risposta al trattamento dopo 8-12 settimane tramite follow-up con esecuzione di spirometria, dosaggio delle IgE sieriche totali e Rx torace. Sono indice di una buona risposta un significativo miglioramento dei sintomi (score di Likert o VAS ³ 50%) e del quadro radiologico, accompagnati da una riduzione delle IgE totali sieriche di almeno il 20%.
3c) Gestione dell’ABPA dipendente dal trattamento
In considerazione dell’alto tasso di pazienti affetti da ABPA che divengono nel tempo dipendenti dal trattamento, in questi casi il consensus consiglia l’impiego di itraconazolo a lungo termine, amfotericina B nebulizzata o farmaci biologici come omalizumab, che trova il suo razionale terapeutico negli elevati livelli di IgE caratteristici dell’ABPA.
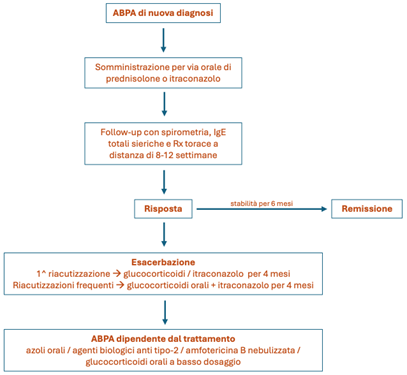
Grafico 1 – Gestione terapeutica dei pazienti affetti da ABPA/M
Conclusioni
In conclusione, le nuove linee guida 2024 offrono un approccio più sistematico e stratificato alla comprensione delle patologie correlate ad Aspergillus, enfatizzando l’importanza di una diagnostica differenziata e di un trattamento personalizzato.
Bibliografia di riferimento
- Agarwal R, Chakrabarti A, Shah A, et al. Allergic bronchopulmonary aspergillosis: review of literature and proposal of new diagnostic and classification criteria. Clin Exp Allergy 2013;43:850-73.
- Agarwal R, Sehgal IS, Muthu V, et al. Revised ISHAM-ABPA working group clinical practice guidelines for diagnosing, classifying and treating allergic bronchopulmonary aspergillosis/mycoses. Eur Resp J 2024;63:2400061.







